□ 省镇江一中 傅靓 王文涛
电能是我们身边最容易得到的能源。手机没电了?只要找到墙边的插座或者插上充电宝,很快就可以充满电。只要找到插座,我们几乎可以获得不间断的能源。但是我们却很少考虑插座里的电是从何而来。在古代,能够自然获得电能就是闪电,但是这种形式的电能是无法直接使用的。近代莱顿瓶的发明让我们可以存储通过摩擦起电产生的少量电能。直到1799年,伏特发明了化学电池后我们才能在科学实验和生活中利用持续的电能。
1.化学电池
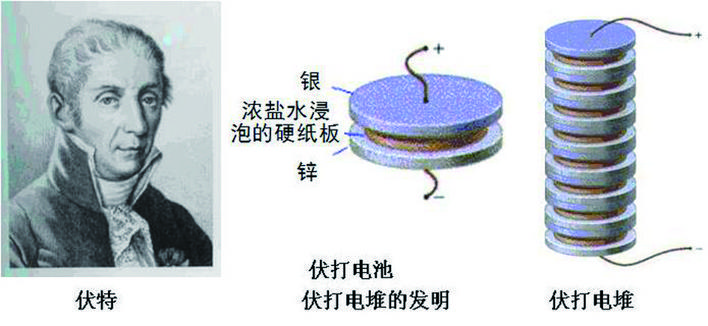
化学电池的发明是人类历史上的一大进步。在电池发明之前,实验室中的电流只能通过摩擦方式产生电荷中和产生。伏特发明了最早的化学电池——伏打电堆,可以提供持续的电流供科学实验。伏打电堆的基本结构是将银片和锌片交错叠放,每层间夹着一层浓盐水浸泡过的纸板。伏打电堆中的银片相当于正极,锌片相当于负极。
正极的反应方程式为:O2+4e-+2H2O=4OH- (还原反应)
负极的反应方程式为:Zn-2e-=Zn2+ (氧化反应)
总反应方程式为:2Zn+O2+2H2O=2Zn(OH)2
由上面的方程式可知:化学电池的本质是指通过氧化还原反应,将化学能转化为电能的一类装置。化学电池中负极发生氧化反应,正极发生还原反应,电子通过外部导线从负极定向移动到正极,从而形成电流。在此过程中,化学能转变为电能。随着化学研究的深入,伏打电堆逐渐小型化,电解液也变为糊状的氯化铵,演变成了我们熟悉的干电池,如锌锰电池、碱性电池。
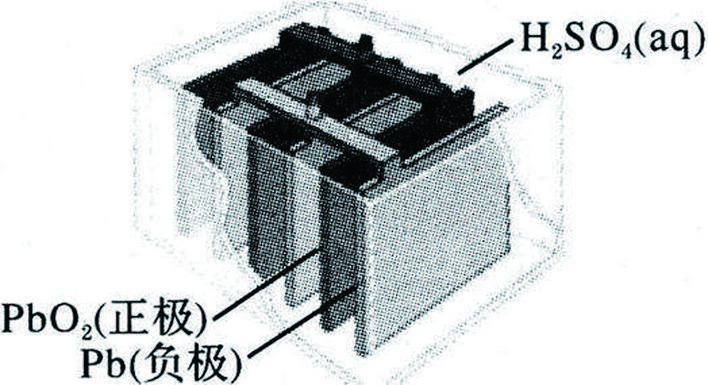
除了上述一次性使用的干电池以外,还有可以重复使用的可充电电池。比如手机和充电宝里中使用比较广泛的锂离子电池,大部分电动自行车中使用的铅蓄电池,电动汽车中比较有发展前途的三元聚合物锂电池等都是可充电电池。以铅蓄电池为例,电池的基本结构如下图所示,其负极为填满海绵状铅的铅板,正极为填满二氧化铅的铅板,并用密度为1.27-1.28g/cm3的稀硫酸作电解质。
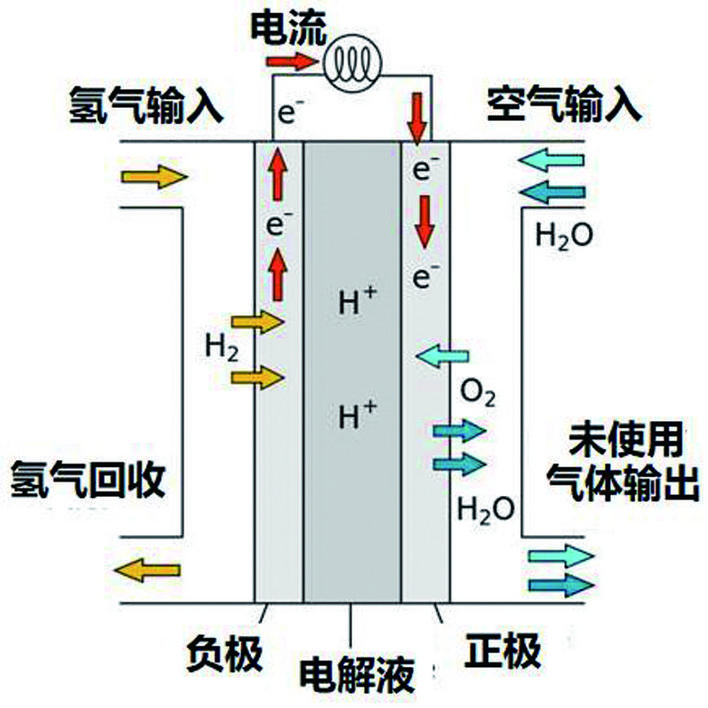
除了上面介绍的两类电池外,还有一类化学电池——燃料电池。燃料电池是一种将燃料的化学能通过电化学反应直接转化成电能的装置,与一般化学电池不同的是反应物不储存在电池内,只在反应时通入电池。以酸性条件下的氢氧燃料电池为例,其原理是利用氢气在负极发生氧化反应,将氢气发生氧化反应得到氢离子,而空气中的氧气在正极发生还原反应,与由负极生成的氢离子结合生成水,其结构原理如图所示。虽然燃料电池仍然通过氧化还原反应过程中产生电流,但是它与前面两种电池的最大区别在于:前面两种电池其反应物在电池内,一旦反应物反应结束,电池就没电了。而燃料电池的反应物放置在电池外部,可以随时添加,电池没电时只需添加反应物即可。
科学家们利用燃料电池原理设计了多种类型的燃料电池,如碱性燃料电池(AFC)、磷酸燃料电池(PAFC)、质子交换膜燃料电池(PEMFC)、熔融碳酸盐燃料电池(MCFC)、固态氧化物燃料电池(SOFC),以及直接甲醇燃料电池(DMFC)等,主要区别就是反应物、电极结构以及电解液有所不同。而其中直接甲醇燃料电池(DMFC),利用甲醇氧化反应作为正极反应的燃料电池技术,很有希望被实用化。
2.核能电池
核能电池(又称原子能电池,放射性同位素发电装置)是指那些使用放射性同位素衰变时产生的能量来产生电力的装置。核电池并非利用核裂变工作的电池,只是利用原子核衰变过程中的热能或者电子产生电流。核电池比起一般电池有很长的寿命且其输出能量远比一般化学电池为高,但其制作成本也相对很高,因此多用于一些需长时间运作又难以更换电池的仪器之上,如卫星、探测器、海底中继器等。
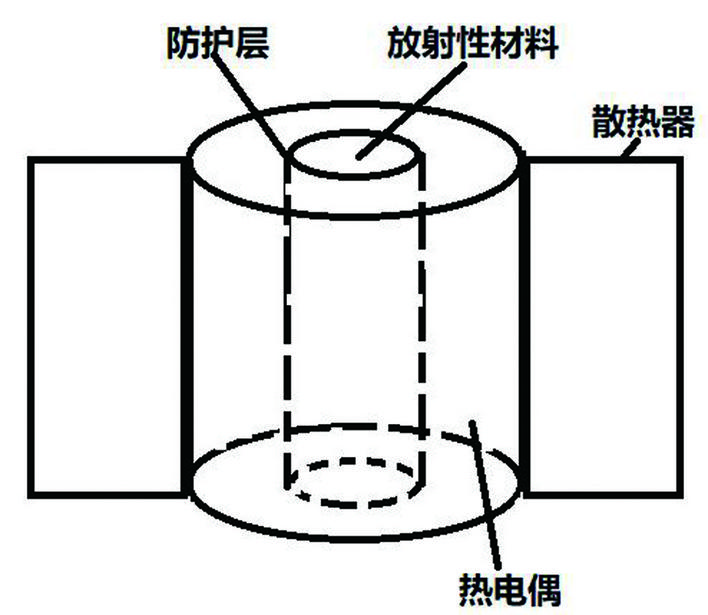
常见的核电池有两大类,一类是宇宙探测等使用的放射性同位素热电发生器(Radioisotope Thermoelectric Generator ,简称为RTG, RITEG),其利用放射性元素衰变时释放的热能,将热能转换为电能。常用的放射性元素为钚238,其衰变方程为:239Pu→235U+4He,由于衰变产物大部分为4He,也就是α粒子,其防护层不需要太厚,便于减轻电池的重量。其原理如下图所示,放射性材料衰变产生的热量在防护层与外界产生温度差,在两层之间的热电偶通过温差发电,将热能转换为电能。右图为好奇号所用的核电池,既可以产生电能,同时多余的热量可以为探测器保温。
第一个离开太阳系的太空探测器“旅行者1号”就是用核电池作为能源,供应电力给探测器上的仪器。从发射算起,已经工作了三十多年,预计可以工作到2025年左右。
核电池的另一类是直接捕获衰变时产生的α或β粒子产生电能,此类装置特点是电压高(可达几十kV),但电流很小(10-11A),其能量利用效率比较高,但是由于电流微弱,现阶段运用的不太广泛,基本停留在实验室研究阶段。
3.光电池
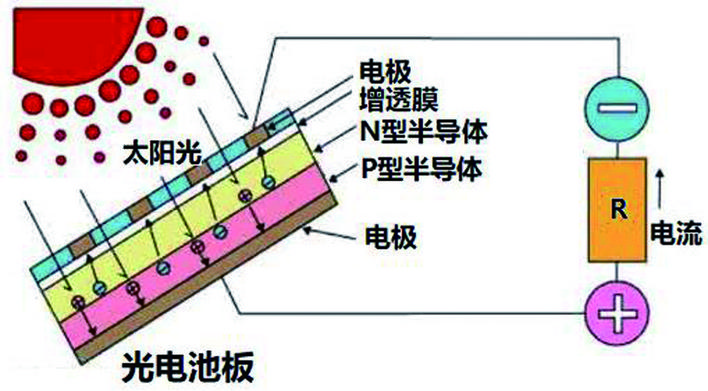
光电池也叫太阳能电池,它的特点是能够把地球从太阳辐射中吸收的大量光能转换成电能。现在我们常用的是硅光电池,它是一种在光的照射下可以直接产生电压的半导体元件。
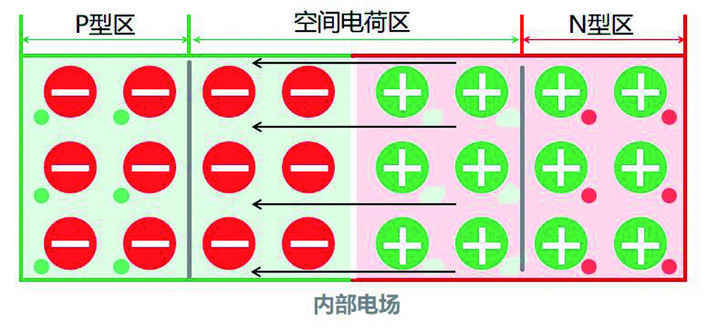
半导体可分为N型半导体(N为Negative的字头,由于电子带负电荷而得此名)和P型半导体(P为Positive的字头,由于空穴带正电而得此名)。N型半导体为含电子浓度较高的半导体,其导电的电荷为自由电子。P型半导体含有较高浓度的“空穴”(“相当于”正电荷),其导电的电荷为“空穴”。P型半导体和N型半导体接触的区域形成PN结,如下图所示。由于扩散作用,P型和N型接触面附近的部分电子和空穴部分结合,在接触层形成一个内部电场。
如果光线照射在太阳能电池上,并且光在PN结被吸收,具有足够能量的光子能够在P型硅和N型硅中将电子从共价键中激发,从而产生电子-空穴对。PN结中产生的电子和空穴对在重新结合中和之前,将被PN结内部电场作用而相互分离。电子跑向带正电的N区,而空穴则向带负电的P区运动,如下图所示。如此正负电荷分别积聚在两端,在P区和N区之间产生电压,如果此时用导线连接两端即可对外供电。
我国76%的国土光照充沛,光能资源分布较为均匀。与水电、风电、核电等相比,太阳能发电没有任何排放和噪声,应用技术成熟,安全可靠。除大规模并网发电和离网应用外,太阳能还可以通过抽水、超导、蓄电池、制氢等多种方式储存,太阳能+蓄能相结合几乎可以满足中国未来稳定的能源需求。
太阳能是未来最清洁、安全和可靠的能源,发达国家正在把太阳能的开发利用作为能源革命主要内容长期规划,光伏产业正日益成为国际上继IT、微电子产业之后又一爆炸式发展的行业。
虽然电池已经诞生200年,但是电池技术还有继续发展的空间,比如现在电动汽车的大量出现就对蓄电池的储能密度和充电速度提出了更高的要求,而燃料电池的发展,尤其是氢燃料电池的发展被认为是兼顾环保和效率的最佳方案,但是氢燃料电池成本高昂,储氢的难度高。所以如何提高电池的能量密度和安全性能,同时降低电池的成本,还有待我们将来继续研究。
负极材料:Pb ,正极材料:PbO2, 电解质溶液:H2SO4
放电时的化学反应:
负极:Pb - 2e- + SO42- = PbSO4
正极:PbO2 + 2e- + SO42- + 4H+ = PbSO4 + 2H2O
总反应:Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O
充电时的化学反应:
阴极:PbSO4 + 2e- = Pb + SO42-
阳极:PbSO4 - 2e- + 2H2O = PbO2 + 4H+ + SO42-
总反应:2PbSO4 + 2H2O = Pb + PbO2 + 2H2SO4